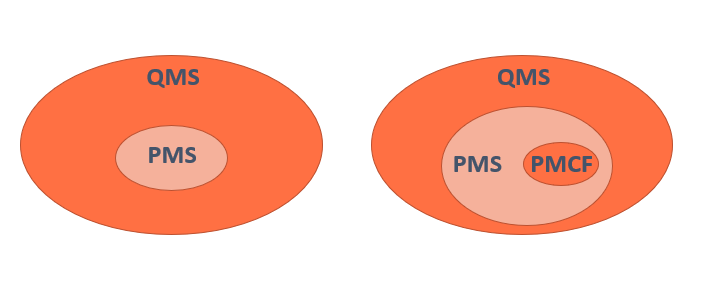
Clasificación del SW según MDR
La regla 11 del MDR y la guía MDCG2019-11 El MDR en su Anexo VIII establece criterios específicos de clasificación para el software y los programas informáticos a través de la regla de clasificación nº 11. Se puede dividir en 3 partes: Estos párrafos se destinan al SW que proporciona información para hacer diagnósticos o … Leer más