Los fabricantes de productos sanitarios deben seguir los procedimientos de evaluación de la conformidad del MDR antes de comercializarlos para demostrar el cumplimiento con los Requisitos Generales de Seguridad y Funcionamiento o GSPR (General Safety and Performance Requirements) del MDR.
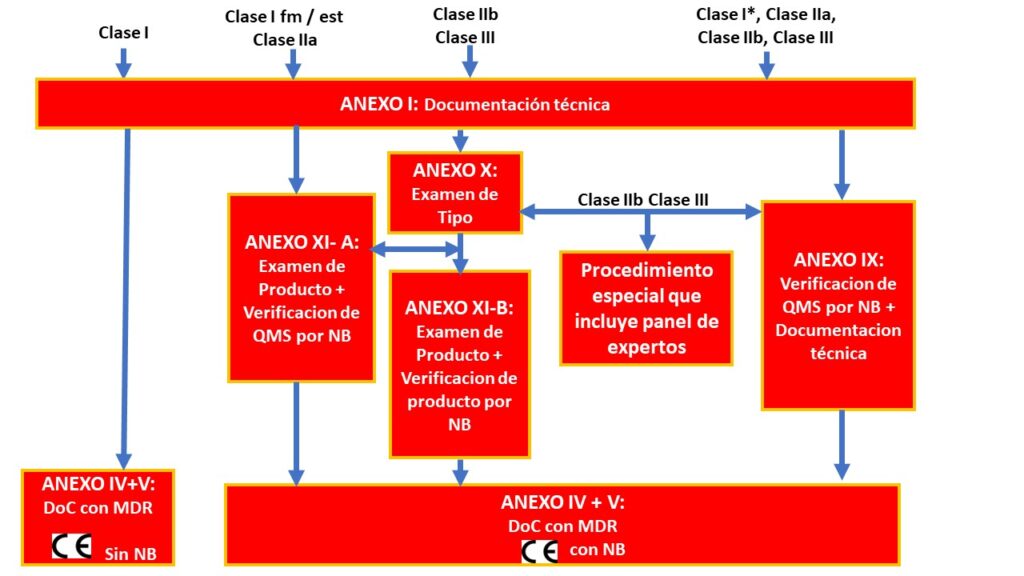
Para productos sanitarios de la clase I, los fabricantes declararán la conformidad con el MDR y colocarán el marcado CE como se describe en los Anexos IV y V.
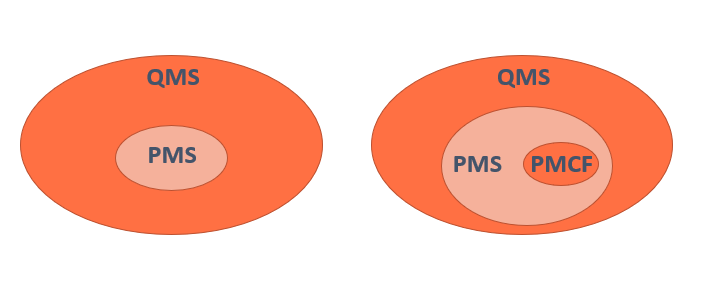
Para los productos que pertenecen a clases superiores, se requerirá un Sistema de Gestión de Calidad o SGC completo, que cumpla con la norma ISO 13485 (Anexo IX). También podrán seguir lo establecido en el Anexo XI.
El Anexo IX ofrece dos alternativas:
- La Parte A describe los requisitos de un SGC para la producción.
- La parte B describe cómo un NB debe verificar la conformidad de cada producto individualmente.
Para productos clase IIb y clase III además es necesario un examen de tipo como se describe en el Anexo X (si no se sigue el Anexo IX). Este examen de tipo significa que el fabricante desarrolla un producto sanitario y antes de producirlo y venderlo, un Organismo Notificado o NB (Notified Body) verifica si se cumplen los GSPR.